水的电离是化学研究中的重要内容。水合氢离子H3O+,是液态水电离产生的独特离子,在维持水的酸碱平衡,包括生命活动在内的许多重要物理化学过程中起着决定性作用。从电子结构上来看,H3O+由H2O分子与一个氢质子以配位键的形式结合,氧原子周围仍剩余一个孤对电子。位于同一周期的C, N元素可以与H以sp3杂化方式键合,形成CH4, NH4+,H3O+原则上可以再吸引一个质子形成水合二氢离子H4O2+。1986年,诺贝尔化学奖得主George A. Olah提出,H4O2+可能作为过渡态存在于氢氚转移过程中,然而由于H3O+和正电荷H+质子之间强静电排斥以及氧周围紧密的电荷排布,迄今为止仍未找到稳定的H4O2+化合物。
目前,高压已被证明是改变元素化学性质的有效工具。在压力作用下,纯水系统将出现复杂的结构相变和超离子态等异常特性。例如,在超过68万大气压下,水冰将相变为具有对称化氢键的X相,具有H4O的局域结构,但不是真正的H4O2+离子;而当压力超过1400万大气压时,由H3Oδ+与OHδ- (δ=0.62)交替组成的离子晶体被预测稳定。在如此高的压力下,H3O+仍未能被进一步质子化,可见形成稳定H4O2+离子所需能量障碍巨大。
据此,bat365在线平台官方网站董校团队提出高压下引入强酸(提供质子过剩环境)可以稳定H4O2+离子相的新途径。课题组团队通过从头算演化结构搜索结合第一性原理计算,预测了高压下H2O-HF系统中多个稳定化合物。在酸性环境中,低温下容易形成稳定的H3O+离子固体,进一步增加压力将迫使H3O+克服H+的斥力,在H4OF2和H5OF3 (H4OF2•HF)化合物中形成H4O单元。质子转移机理、化学键拓扑性质和Bader电荷转移的详细分析提供了有力的证据,支持酸性环境和压力的协同作用下H4O2+的形成。此外,从头算分子动力学模拟揭示了在不同温度下这些离子相的有趣行为,酸性分子的加入(或质子的引入)将使氢原子在比纯水冰系统更低的温度下更早扩散,即,提早进入超离子态。值得注意的是,在H4OF2•HF相中还出现了塑晶态,其中H4O2+表现出与H2O和NH3分子一致的自由转子行为。配位数分析进一步解释了即使在高温区(超离子态区域和流体区域),H4OF2中的大部分瞬态碎片都含有H4O2+离子。尽管实验验证仍然是下一步的关键,但这些研究结果挑战了已建立的理论,如价壳电子对排斥模型、质子转移动力学和酸碱理论,不仅扩展了对基本化学原理的理解,也代表了对极端条件下分子行为理解的范式转变。
相关成果以H4O2+ ion stabilized by pressure为题发表在Phys Rev B期刊上,该工作得到了国家自然科学基金项目资助。
据了解,董校团队已在极端条件下的新规律、新物质和新应用方面取得系列重要进展,相关工作相继发表在Nature、Nature Chemistry、Physical Review Letters、Angewandte Chemie、PNAS等高水平期刊上。
论文链接网址:https://link.aps.org/doi/10.1103/PhysRevB.109.174102
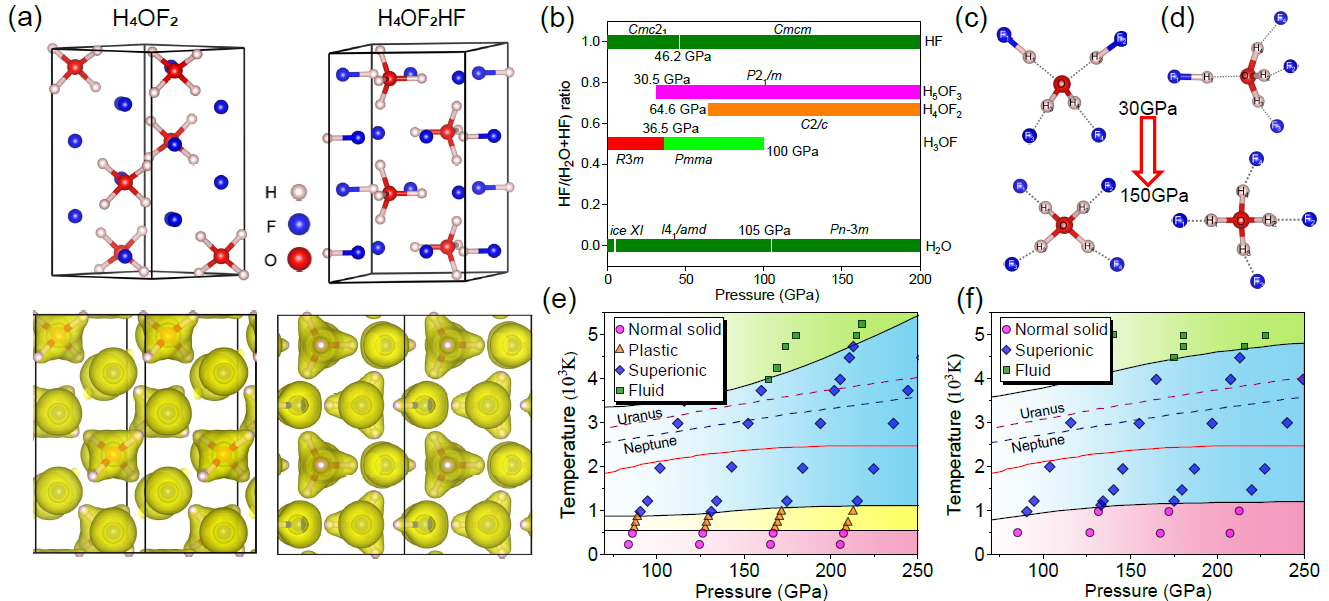
图(a)H4OF2, H4OF2HF的晶体结构和电子局域函数图;图(b)H2O-HF体系压力组分相图;图(c)(d)H4OF2和H4OF2HF结构压力下质子转移示意图;图(e)(f)H4OF2, H4OF2HF温度压力相图。
编校:程丹
审核:薄方





